媒介昆虫-病毒互作组揭示Toll免疫通路介导植物病毒在媒介昆虫体内持久性传播的稳态机制
https://mp.weixin.qq.com/s/I5MjSnnRJ9HOGzOyQ6TFCQ
在长期进化过程中,虫媒病毒已经发展出各种策略来对抗宿主的先天免疫防御,以维持其持续传播。最近的研究表明,除了细菌和真菌外,无脊椎动物的Toll免疫系统在抵御病毒侵染过程中同样具有重要作用,但Toll免疫途径在维持植物病毒在媒介昆虫体内持久增殖过程中的功能目前还未知。
近日,宁波大学陈剑平团队媒介昆虫-病毒互作组揭示了灰飞虱Toll免疫通路的转录因子Dorsal通过调控新的靶标基因,进而激活下游的免疫防御通路抵抗水稻条纹病毒(Rice stripe virus,RSV),同时RSV利用非结构蛋白NS4抑制Dorsal磷酸化从而削弱宿主Toll免疫通路的稳态机制。研究成果以“Maintenance of Persistent Transmission of a Plant Arbovirus in its Insect VectorMediated by the Toll-Dorsal Immune Pathway”为题在线发表在国际著名学术期刊The Proceedings of the National Academy of Sciences(PNAS)上。

在该研究中,作者首先检测了在RSV侵染灰飞虱后的不同时间点Dorsal的表达情况。结果表明Dorsal被显著激活表达。进一步通过RNAi沉默灰飞虱中的Dorsal,发现RSV的积累量显著增加,灰飞虱的获毒率和传毒率也明显上升。同时,RSV侵染后进入细胞核的p-Dorsal水平明显增加。这些结果均表明转录因子Dorsal具有抗RSV的功能。
随后,作者利用ChiP-Seq测序和酵母单杂明确了Dorsal与锌指蛋白ZN708具有很强的结合能力。RNAi实验结果表明转录因子Dorsal正调控靶标基因ZN708。为明确ZN708在RSV侵染过程中的功能,作者沉默灰飞虱中的ZN708并注射RSV粗提液,发现RSV的积累量在注射后的3dpi和6dpi显著增加,同时灰飞虱的获毒率和传毒率明显上升。这些结果均表明ZN708也参与了宿主针对RSV的防御。
为探究Dorsal-ZN708调控的下游免疫防御通路,作者通过沉默Dorsal 和ZN708后的转录组差异分析发现自噬和外泌体通路可能在抵御RSV的过程中发挥重要作用。进一步的实验表明ZN708与自噬蛋白Atg8存在互作,同时Dorsal-ZN708通路正调控关键自噬基因的表达。
为应对灰飞虱的抗病毒免疫,RSV发展了相应的反防御策略。研究表明RSV的非结构蛋白NS4与Dorsal功能域RHD-n存在互作。通过竞争性结合实验、RNAi及纯化蛋白注射等方法发现NS4与MSK2激酶竞争性结合Dorsal从而抑制其磷酸化,进而帮助病毒反防御宿主的Dorsal-ZN708抗病毒过程。
综合以上结果,该研究提出Toll免疫通路介导植物病毒在媒介昆虫中稳态的新机制。宿主抗病毒免疫机制:灰飞虱的Toll受体与RSV的外壳蛋白NP互作并且激活下游的转录因子Dorsal发生磷酸化入核,正调控靶标基因ZN708进而激活自噬等抗病毒免疫通路。病毒反防御机制:RSV利用其非结构蛋白NS4与MSK2激酶竞争性结合抑制Dorsal磷酸化进行反防御,从而实现RSV在灰飞虱体内的持久性增殖及在田间的扩散传播。
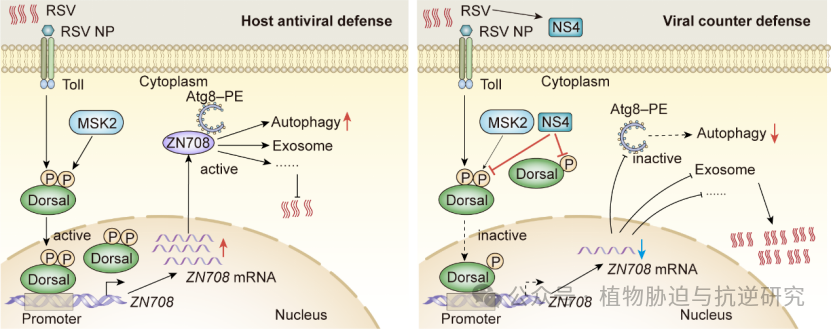
Toll免疫通路介导植物病毒在媒介昆虫中稳态的新机制
论文第一作者为宁波大学植物病毒学研究所博士后何雨娟,通讯作者为张传溪教授、陈剑平院士和李俊敏研究员。该项研究得到了国家自然科学基金重点项目-区域创新联合发展基金(U20A2036)、国家自然科学基金面上项目(32270146)、国家重点研发计划(2021YFD1401100)和宁波大学王宽诚基金资助。
全文链接:https://www.pnas.org/doi/10.1073/pnas.2315982121
| 我也说两句 |
| 版权声明: 1.依据《服务条款》,本网页发布的原创作品,版权归发布者(即注册用户)所有;本网页发布的转载作品,由发布者按照互联网精神进行分享,遵守相关法律法规,无商业获利行为,无版权纠纷。 2.本网页是第三方信息存储空间,阿酷公司是网络服务提供者,服务对象为注册用户。该项服务免费,阿酷公司不向注册用户收取任何费用。 名称:阿酷(北京)科技发展有限公司 联系人:李女士,QQ468780427 网络地址:www.arkoo.com 3.本网页参与各方的所有行为,完全遵守《信息网络传播权保护条例》。如有侵权行为,请权利人通知阿酷公司,阿酷公司将根据本条例第二十二条规定删除侵权作品。 |
 m.quanpro.cn
m.quanpro.cn